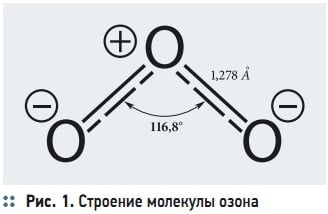
Рис. 1. Строение молекулы озона
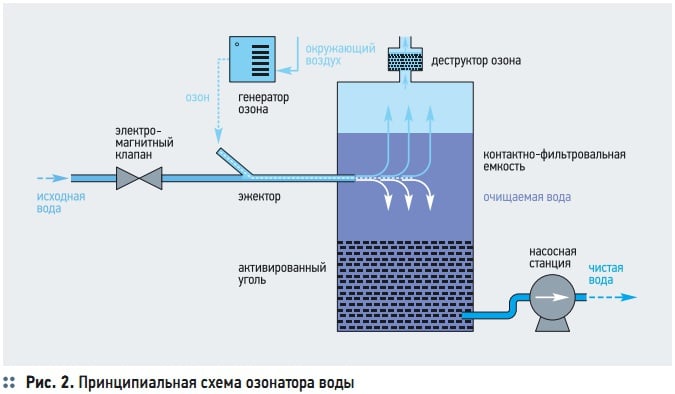
Рис. 2. Принципиальная схема озонатора воды
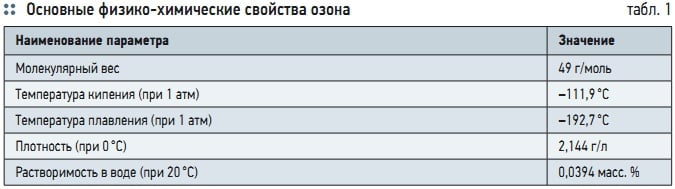
Табл. 1. Основные физико-химические свойства озона
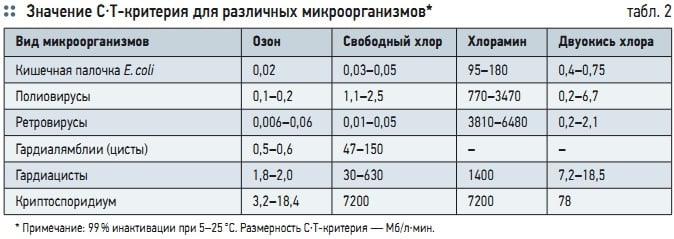
Табл. 2. Значение С⋅Т-критерия для различных микроорганизмов*
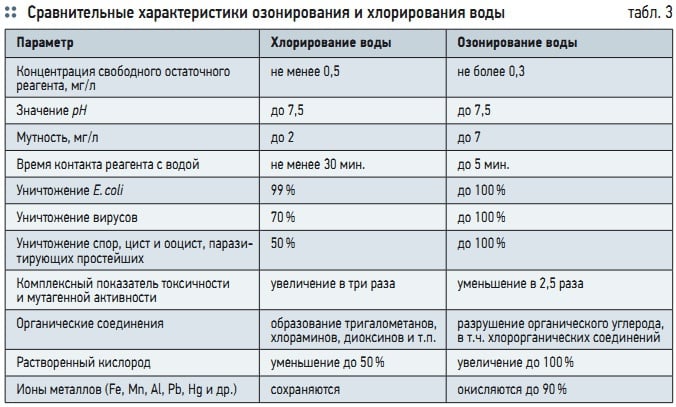
Табл. 3. Сравнительные характеристики озонирования и хлорирования воды
Озонирование воды перспективно в водоподготовке питьевой воды и в водоочистке, используемой в хозяйственных нуждах, для очистки и дезинфекции сточных вод, оборотной воды бассейнов, обеззараживании воды, предназначенной для бутилирования, удаляя из воды неприятные привкусы и запахи, а также используется для дезинфекции производственных и бытовых помещений и дезодорации воздуха.
В данной статье рассмотрены основные аспекты применения озона в водоподготовке. Очистка и получение пригодной для потребления питьевой воды является важным этапом водоподготовки. По традиционной схеме водоподготовка обычно включает три основных стадии: механическую фильтрацию, удаление из воды взвешенных и коллоидных веществ (осветление) и обеззараживание [1]. Удаление из воды взвесей достигается при помощи сорбционных методов и фильтров.
Для осветления воды применяется химическая обработка специальными коагулянтами (сернокислый алюминий Аl(SO4)3⋅18Н2О, сернокислое железо FeSO4⋅7Н2О, хлорное железо FeCl3⋅6H2O), способными осаждать коллоидные частицы гидроксидов железа или алюминия с адсорбированными на них коллоидами загрязнений, размером до 0,07 мк [2]. Для обеззараживания воды используется обработка хлором и его производными (окись хлора (ClO2), гипохлорид натрия NaOCl), содержащими 95–97 % активного хлора [3].
Необходимость использования трех различных процессов существенно усложняет технологию обработки воды. Из-за значительной стоимости сорбционных установок и сложности технологического процесса водоподготовки часто приходится пренебрегать улучшением вкусовых качеств воды. Кроме этого, при обработке воды коагулянтами в воду поступают дополнительные загрязнения; хлорирование, в свою очередь приводит к образованию в воде токсически опасных хлорорганических соединений.
Альтернативным хлорированию способом в водоподготовке является обработка воды озоном. Озон — газ синего цвета с характерным резким запахом, образующийся при воздействии электрического разряда или ультрафиолетового излучения на воздух [4]. При низких температурах (–112 °С) озон превращается в темно-синюю жидкость, при более глубоком охлаждении образует темно-фиолетовые кристаллы (tпл = 192,7 °C, tкип = 111,9 °C, растворимость в воде при 20 °C равна 0,0394 масс. % — табл. 1).
Озон применяется в очистке и доочистке питьевой воды, подготовке воды для производства пива, безалкогольной и слабоалкогольной продукции, стерилизации стеклянных и пластиковых (ПЭТ) бутылок, озонирования воды в бассейнах и аквариумах, санации стоков, дезинфекционной обработке помещений любого типа и др. По степени опасности озон относится к первому классу вредных веществ: максимальная разовая предельно допустимая концентрация (ПДК м.р.) озона в атмосферном воздухе населенных мест — 0,16 мг/м3; среднесуточная ПДК (ПДК с.с.) озона в атмосферном воздухе населенных мест — 0,03 мг/м3; ПДК озона в воздухе рабочей зоны составляет 0,1 мг/м3.
По химическому строению озон представляет собой молекулу, состоящую из трех атомов кислорода с длиной связи 1,278 А ° и валентным углом 116,8° (рис. 1). Молекула озона полярна, ее дипольный момент 0,534D. Озон неустойчив и при нормальных условиях (20 °C, 1 атм) самопроизвольно превращается в кислород O2 с генерированием атомарного кислорода и выделением тепла. Период полураспада озона в воздухе составляет 30– 40 мин.
Повышение температуры и понижение давления увеличивают скорость перехода озона О3 в O2. При больших концентрациях О3 процесс может носить взрывной характер. Контакт озона даже с малыми количествами органических веществ, некоторыми металлами или их оксидами ускоряет превращение О3 в O2. Озон — сильный окислитель и со многими непредельными органическими соединениями образует озониды — промежуточные продукты присоединения озона по двойной связи [5].
Первичным продуктом взаимодействия озона является малозоид (1, 2, 3-триоксолан), который неустойчив и распадается на карбонилоксисид [> C = O–O]* и карбонильные соединения — альдегиды или кетоны. Реакция озонирования чрезвычайно экзотермична, избыток тепла уходит на электронно-колебательное возбуждение образующихся продуктов реакции и частично рассеиваются молекулами растворителя. Промежуточные продукты, образующиеся в этой реакции, вновь реагируют в другой последовательности, образуя озониды.
В присутствии веществ, способных вступать в реакцию с карбонилоксидом (спирты, кислоты), вместо озонидов образуются различные перекисные соединения. Озон активно вступает в реакцию с ароматическими органическими соединениями, при этом реакция идет как с разрушением ароматического ядра, так и без его разрушения [6]. При взаимодействии озона с фенолами происходит образование соединений с нарушенным ароматическим ядром (типа хиноина), а также малотоксичных производных непредельных альдегидов и кислот.
В реакциях с насыщенными углеводородами, протекающих как в водных растворах, озон вначале распадается с образованием атомарного кислорода, который инициирует цепное окисление [7]. При этом выход продуктов окисления соответствует уровням расхода озона. Озон также способен взаимодействовать с щелочными металлами — натрием Na, калием K, рубидием Rb, цезием Cs, посредством формирования промежуточного неустойчивого комплекса катиона металла с озоном [М+–О–Н+–O3 – ]*, в результате последующего водного гидролиза которого образуется смесь озонида МО3 и водного гидроксида щелочного металла (MOH) [8].
Озон — сильный дезинфектант, оказывающий выраженное бактерицидное воздействие на многие патогенные микроорганизмы, бактерии и вирусы. При оценке эффективности озона используется С⋅Т-критерий, т.е. произведение концентрации реагента на время его действия. По своему дезинфицирующему действию озон превосходит хлор, хлорамин и двуокись хлора (табл. 2).
Из-за высокой окислительной способности озон действует как сильный окислитель на клеточную стенку мембран микроорганизмов с последующим проникновением внутрь клетки и окислением жизненно важных биологически активных соединений (белки, ферменты, ДНК, РНК) [9]. Благодаря своим окислительным свойствам озон уничтожает бактерии в три-пять раз эффективнее УФ-излучения и в 500–1000 раз сильнее хлора.
Озон более эффективен, чем хлор, при уничтожении кишечной палочки Еcherihia coli, которая в воде уничтожается озоном в 1000 раз быстрее, чем хлором [10]. Время, необходимое для уничтожения Endamoeba hystolica при остаточной концентрации озона в воде 0,3 мг/л, составляет 2–7,5 мин., а для хлора (ост. концентрация 0,5–1 мг/л) — 15–20 мин. Вирус полиомиелита уничтожается озоном за две минуты при концентрации 0,45 мг/л, тогда как при обработки воды хлором в концентрации 1 мг/л для этого требуется три часа [11].
Все эти вышеперечисленные факторы способствуют применению озона в водоподготовке, имеющей ряд неоспоримых преимуществ по сравнению с другими существующими технологиями, в т.ч. хлорированием воды (табл. 3). Важным преимуществом является неспособность озона в отличие от хлора, к реакциям замещения с органическими соединениями, приводящими к образованию побочных токсичных хлорорганических соединений — тригалометанов, главным представителем которых является хлороформ (СHCl3) [12].
Показано, что в процессе хлорирования воды может образовываться до 50-ти различных галогенсодержащих соединений, включая бромоформ (СHBr3), дибромхлорметан (CHBr2Cl), бромдихлорметан (CHBrCl2), и хлороформ (СHCl3) [13]. Озонирование в водоподготовке не приводит к образованию тригалометанов и за счет высокой окислительной способности озона позволяет одновременно достичь осветления воды и осаждения примесей, а также устранить привкусы и запахи при обеззараживании.
По многим характеристикам, включая комплексный показатель токсичности и мутагенной активности, озон превосходит хлор и его производные (табл. 2). При растворении в воде озон разлагается на О2 с генерированием реакционно-способного атомарного кислорода, способного быстро окислять загрязнения органической и неорганической природы, переводя их из растворенного состояния во взвеси, задерживаемые сорбционным фильтром [14].
По современной технологии производство озона осуществляется на месте потребления на специальных установках — озоногенераторах, генерирующих озон при высокочастотном коронном разряде в потоке осушенного воздуха. Расход энергии при этом процессе составляет 5–15 кВт/(кг О3⋅ч), концентрация озона в воздушно-озонной смеси выходит примерно 50–250 г/м3. Полученный таким способом озон, затем подается в систему водоподготовки за счет методов барботажа и инжекции.
В крупных промышленных установках наиболее часто используется барботаж озоно-воздушной смеси через очищаемую воду. При этом, важным технологическим этапом является обеспечение одинакового времени контакта газообразного озона с водой, а также равномерное введение его по всему объему обрабатываемой воды. В установках относительно небольшой производительности по озону наиболее распространен и достаточно эффективен метод инжекции.
Очищаемая вода проходя через инжектор, создает в нем разрежение, при котором в воду поступает необходимое количество газообразного озона. Интенсивное перемешивание в инжекторе диспергирует озон на мельчайшие пузырьки с большой поверхностью контакта, тем самым повышая скорость растворения озона в воде. Совместить эффективное растворение озона и время его контактирования с водой позволяют пульсационные колонны со специальными распределительными тарелками.
Озоно-воздушная смесь поступает в нижнюю часть колонны; возвратно-поступательное движение воды, создаваемое специальным пульсатором, и распределительные тарелки обеспечивают ее диспергирование до пузырьков заданных оптимальных размеров, которые поднимаются противотоком к двигающемуся вниз потоку воды. В результате этого процесса достигается высокая степень дисперегирования озона при большой удельной производительности аппарата.
После растворения озона в воде необходимо обеспечить нужное время его контакта с водой для осуществления химических реакций окисления и удаления из воды избыточного количества непрореагировавшего озона и продуктов распада. Для этого применяется контактнофильтровальный аппарат, из которого вода направляется на фильтр на основе активированного угля для каталитического окисления продуктов взаимодействия озона с органическими соединениями с последующей их задержкой фильтром и деструкцией озона (рис. 2).
Применение современных передовых технологий производства озона позволяют создавать малогабаритные, надежные, высокопроизводительные и легкие в наладке и обслуживании отечественные системы озонирования воды, снабженные датчиками электронного контроля и системами регулирования.
Заключение
Преимущества озона по сравнению с технологией хлорирования заключаются в следующих факторах: озон экологически безопасен и не образует токсичных побочных продуктов распада; остаточный озон быстро превращается в кислород; озон вырабатывается на месте, не требуя хранения и перевозки; озон уничтожает все известные микроорганизмы: вирусы, бактерии, грибы, споры, цисты, простейших и т.д. в 300–1000 раз быстрее, чем др. дезинфектанты; не существует и не может возникнуть устойчивых к озону форм микробов; обработка воды озоном занимает несколько минут; озонирование удаляет из воды неприятные запахи и привкусы; одновременно с обеззараживанием происходит осветление воды. К недостаткам озона следует отнести сложность его производства на месте использования, необходимость значительных энергозатрат, связанных с его получением, а также недостаточно высокую устойчивость озона в воде, разлагающегося в ней в течении 30–40 минут.
























