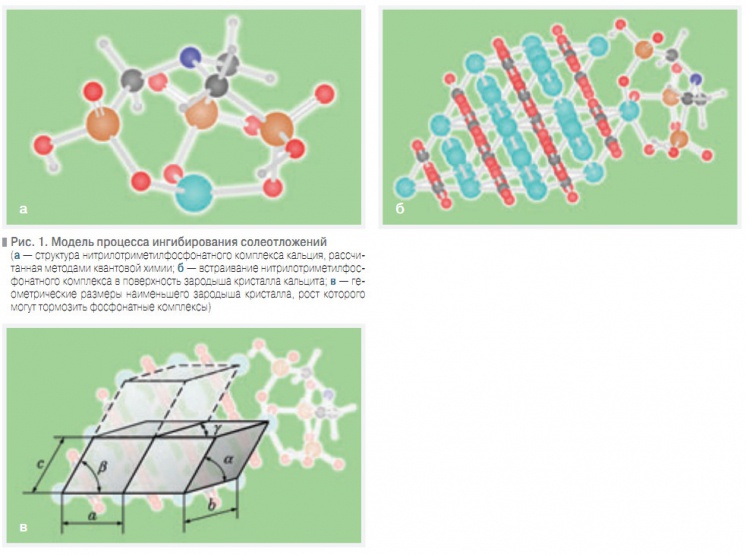
Рис. 1. Модель процесса ингибирования солеотложений
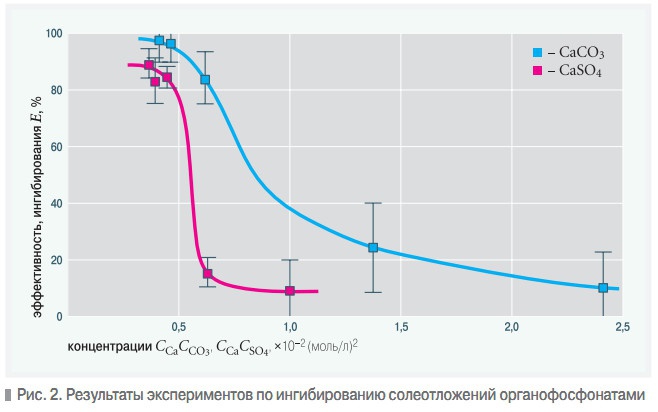
Рис. 2. Результаты экспериментов по ингибированию солеотложений органофосфонатами
Введение
Применение производных органофосфоновых кислот в качестве ингибиторов коррозии и солеотложений было впервые предложено и запатентовано специалистами США в 1960-х гг. [1, 2]. Вслед за этим во многих странах были разработаны разнообразные технологические процессы противонакипной и противокоррозионной обработки воды, основанные на введении в воду органофосфоновых кислот и их производных. Однако механизм действия этих препаратов длительное время оставался невыясненным.
Анализ взаимодействия фосфоновых кислот и других комплексонов с ионами солей, образующих отложения, был проведен Н.М. Дятловой и др. [3]. Точка зрения, что ингибирующее действие фосфонатов обусловлено их адсорбцией на поверхности растущих кристаллов минеральных солей, в дальнейшем получила подтверждение.
Однако предложенная в работе [4] математическая модель влияния фосфоновых кислот на процессы кристаллизации минеральных солей представляется неубедительной, так как в ней не учтены основные факторы — структура поверхности и механизм роста кристаллов минеральных солей. Позднейшие исследования [5, 6] показали, что ингибирующей активностью обладают не сами комплексоны, а их соединения с ионами металлов — комплексонаты.
Российскими учеными разработаны ингибиторы солеотложений и коррозии на основе комплексных соединений органофосфоновых кислот с цинком [7, 8, 9]. Несмотря на развитие представлений о механизме действия ингибиторов солеотложений, строгие критерии их применимости в конкретных условиях до последнего времени отсутствовали. Это приводило к многочисленным трудностям и неудачам при использовании комплексонных препаратов для противонакипной обработки воды [10, 11, 12].
Основной вопрос при использовании фосфонатов для противонакипной обработки воды стоит о том, каково предельно допустимое содержание в воде ионов соли, образующей отложения, при котором фосфонатная обработка еще способна предотвратить кристаллизацию минеральных солей. Так как основной солью, образующей отложения, чаще всего бывает карбонат кальция, то в качестве критериев применимости фосфонатов в энергетике традиционно рассматривают кальциевую жесткость ЖCa, щелочность Щ (определяемая содержанием, в основном, карбонат- и гидрокарбонат-анионов) или их произведение ИК = ЖCaЩ, называемое карбонатным индексом.
Значения ЖCa и Щ обычно принято выражать в мг-экв/л, а ИК — в (мг-экв/л)2. Первоначально Научно-техническим советом РАО «ЕЭС России» было рекомендовано [13] ограничить применение комплексонатной обработки воды предельно допустимым значением ИК = 8 (мг-экв/л)2. На основе практического опыта применения фосфонатной обработки воды автором данной статьи были даны рекомендации [14] по применению фосфонатов при значениях ИК до 50 (мг-экв/л)2.
Позже Балабан-Ирменин и др. [15] подвергли критике эти ограничения, указав на возможность применения комплексонатной обработки воды при еще более высоких значениях ИК даже при меньших дозировках ингибитора. Другим серьезным вопросом является влияние максимально допустимой температуры воды (с учетом пристенных перегревов в котле или теплообменнике), при которой органофосфонаты способны ингибировать солеотложения.
Современные теоретические основы ингибирования кристаллизации минеральных солей, позволяющие получить ответы на эти вопросы, развиты в работе [16].
Теоретическое обоснование предлагаемого способа
Способ ингибирования солеотложений основан на введении в воду органофосфоновых кислот, их солей или комплексов с металлами. При введении кислот, например, нитрилотриметилфосфоновой кислоты, молекулы кислоты в водном растворе подвергаются ионизации
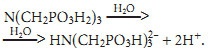
Аналогично подвергаются ионизации и молекулы солей этих кислот. Образовавшиеся ионы взаимодействуют с содержащимися в воде ионами кальция и других металлов с образованием комплексных соединений — фосфонатов:
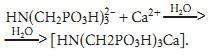
Строение фосфонатов хорошо изучено.В качестве примера на рис. 1а приведена схема строения иона нитрилотриметилфосфоната кальция, рассчитанная известным в квантовой химии полуэмпирическим методом CNDO при помощи программы HyperChem. В состав наиболее эффективных современных ингибиторов солеотложений входят уже готовые фосфонаты металлов, чаще всего цинка.
Ионы фосфонатов, обладающие большим дипольным моментом, адсорбируются на поверхности зародышей кристаллов. В результате зародыши, находящиеся вблизи границы термодинамической устойчивости, не могут расти и растворяются под влиянием флуктуаций, обусловленных тепловым движением. Механизм образования зародышей кристаллов в пересыщенном растворе минеральных солей до настоящего времени однозначно не выяснен.
Это не дает возможности обосновать ингибирование солеотложений строгими расчетами. Однако очевидно, что рост кристалла возможен только из такого зародыша, который обладает основными элементами симметрии кристаллической решетки минеральной соли. Поэтому далее мы дадим оценку порядка величин, ограничивающих область эффективного ингибирования солеотложений фосфонатами.
Для этого предположим, что зародыш кристалла состоит из нескольких сформированных ячеек кристаллической решетки минеральной соли, а рост такого зародыша осуществляется застройкой соседних ячеек, образующих ступени роста на поверхности зародыша. Адсорбция иона фосфоната на поверхности такого зародыша не дает возможности застроить частицами минеральной соли примыкающие ячейки кристаллической решетки и вследствие этого тормозит рост зародыша (рис. 1б).
Очевидно, что адсорбция ионов фосфоната может тормозить только рост зародыша, но никак не его первоначальное флуктуационное возникновение. Для того, чтобы тормозить рост зародыша, адсорбированный ион фосфоната должен занять положение, пересекающее границы примыкающей к поверхности зародыша соседней ячейки кристаллической решетки. Для этого зародыш должен иметь хотя бы одну минимально развитую грань.
Это возможно только в том случае, если зародыш состоит, как минимум, из двух ячеек кристаллической решетки (рис. 1в).С другой стороны, введение фосфонатов в воду может предотвратить кристаллизацию минеральных солей только в том случае, когда такой зародыш термодинамически неустойчив. Такой зародыш будет находиться в неустойчивом равновесии с раствором, если при его образовании изменение изобарно-изотермического потенциала (свободной энергии Гиббса) ∆G будет положительным [17]. Значение ∆G дается формулой
∆G = Sσ– N∆μ, (1)
где S — поверхность зародыша, м2; σ—свободная энергия поверхности, Дж/м2; N— число формульных единиц соли в зародыше; ∆μ— разность химических потенциалов соли, образующей отложения, в растворе и в кристалле. Из рис. 1в видно, что поверхность зародыша составляет
S = 4absinγ+ 4acsinβ+ 2bcsinα,(2)
где a, b, c — длины ребер ячейки кристаллической решетки, м; α, β, γ— углы между ребрами ячейки кристаллической решетки. Число формульных единиц соли в зародыше
N= 2n, (3)
где n — число формульных единиц соли, образующей отложения, в одной ячейке кристаллической решетки. Разность химических потенциалов ∆μ дается формулой
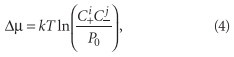
где k — постоянная Больцмана, k = 1,38 •10–23 Дж/К; T — абсолютная температура, К; C+ — концентрация в воде катиона соли, моль/л; i — число катионов в формуле соли; C– — концентрация в воде аниона соли, моль/л; j — число анионов в формуле соли; P0 — произведение растворимости соли (зависящее от температуры). Подставив в формулу (1) формулы (2), (3) и (4), из неравенства получим условие эффективного ингибирования солеотложений:
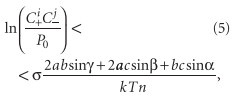
Подставляя в формулу (5) соответствующие параметры конкретных минеральных солей (хорошо известные из справочных данных), можно получить условия, при которых фосфонатная обработка воды может быть эффективной по отношению к определенным солям. Например, при температуре 300 К (27°C) эффективное предотвращение солеотложений карбоната кальция возможно только при условии
CCaCCO3 < 6,5•10–3 (моль/л)2, (6)
где CCa — концентрация ионов кальция, моль/л;CCO3 — концентрация карбонат-ионов, моль/л; а сульфата кальция — при условии
CCaCSO4 < 4,7•10–3 (моль/л)2, (7)
где CSO4 — концентрация сульфат-ионов,моль/л. При повышении температуры указанные границы резко снижаются — как из-за увеличения знаменателя правой части неравенства (5), так и за счет уменьшения произведений растворимости указанных солей. Кроме того, полученные соотношения дают только теоретический предел, и все изложенное совершенно не означает, что во всех случаях, когда (5)–(7) выполняются, применение фосфонатов технически эффективно и экономически оправданно. Однако если эти условия не выполнены, то ингибирование солеотложений фосфонатами вообще невозможно.
Экспериментальная проверка
Для проверки описанного способа были проведены серии экспериментов по ингибированию кристаллизации карбоната и сульфата кальция при температуре 300±5 К и различных концентрациях ионов, образующих эти соли. Для изучения кристаллизации карбоната кальция в воду вводили хлорид кальция по ТУ 6-09-3834–80, карбонат натрия по ГОСТ 83–79 и ингибитор— оксиэтилидендифосфоновую кислоту по ТУ 2439-363-05763441–2002. При исследовании кристаллизации сульфата кальция использовали хлорид кальция, сульфат натрия по ГОСТ 6318–77 и ингибитор — нитрилотриметилфосфоновую кислоту по ТУ 2439-34705763441–2001. В обоих случаях за критерий эффективности ингибирования принималась величина
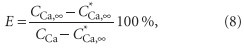
где CCa, ∞— установившаяся концентрация ионов кальция после выпадения осадка, моль/л; C*Ca, ∞— установившаяся концентрация ионов кальция после выпадения осадка в контрольном опыте (без добавления ингибитора),моль/л. На рис. 2 приведены зависимости эффективности ингибирования кристаллизации указанных солей от величин CCaCCO3 и CCaCSO4.Можно видеть, что в интервале значений: CCaCCO3< 6,5•10–3 (моль/л)2 эффективность ингибирования остается достаточно высокой для практического использования описанного способа.
При значениях же CCaCCO3> 6,5•10–3 (моль/л)2 эффективность ингибирования не превышает 16%, а с учетом ошибок эксперимента может быть даже равна нулю. Аналогично, при CCaCSO4< 4,7•10–3 (моль/л)2 эффективность ингибирования сульфата кальция остается достаточно высокой, если же CCaCSO4 >4,7•10–3 (моль/л)2, то введение ингибитора даже в повышенных концентрациях не дает приемлемого результата. Приведенные результаты в целом подтверждают изложенные теоретические доводы и доказывают практическую применимость описанного способа.
Практическое применение технологии
Описанный способ предотвращения солеотложений успешно применен автором на многих объектах теплоэнергетики как в Удмуртской Республике, так и в других регионах России. На практике контроль концентрации ионов солей, образующих отложения, осуществляют предварительно, перед введением в воду фосфоновых кислот или их производных, а также периодически, в процессе обработки воды фосфонатами.
Для определения концентрации ионов используют известные в аналитической химии и хорошо зарекомендовавшие себя способы — титриметрический, электрохимический или фотоколориметрический. В ряде случаев при исследовании состава исходной воды и режимов работы теплоэнергетического оборудования оказывается, что перед введением фосфонатов ее необходимо подвергнуть предварительной обработке для снижения концентрации ионов соли, образующей отложения, до тех пор, пока условия (5)–(7) не будут выполнены.
Такая предварительная обработка тоже не требует сложных технических средств. Как правило, для этого используют имеющееся на котельной технологическое оборудование, например, первую ступень ионообменных фильтров, деаэратор, декарбонизатор или систему подкисления воды серной или фосфорной кислотой. Для введения в воду фосфоновых кислот или их производных с успехом применяются дозировочные насосы или эжекторные установки.
Положительно зарекомендовали себя дозировочные насосы типа «НД», выпускаемые ЗАО «Дозировочные насосы и системы» (г. Тула) и дозировочные насосы фирмы Grundfos (Дания). В последнее время специалистами ООО «Экоэнерго» разработан отечественный мембранный дозировочный насос «ЭКО-1». Для теплотехнических объектов средней и малой мощности оптимальным решением является малогабаритное и эффективное эжекционное дозирующее оборудование, разработанное автором: дозаторы «Иж-25М», «Импульс», «Комплексон» и «Ижик».
В результате практического применения и многолетнего опыта эксплуатации водогрейных и паровых котельных с использованием описанного способа обработки воды удалось добиться практически полного отсутствия солеотложений, а также, благодаря использованию цинковых комплексов оксиэтилидендифосфоновой и нитрилотриметилфосфоновой кислот, значительно снизить интенсивность коррозии теплоэнергетического оборудования.
Авторские и патентные права
Описанный способ ингибирования солеотложений признан изобретением и защищен патентом Российской Федерации по заявке №2005127830, выданным на имя автора. Согласно ст. 10 Патентного Закона РФ и ст. 1358 Гражданского Кодекса РФ, этот патент предоставляет автору исключительное право использовать описанный способ, а также выдавать разрешения (лицензии) на такое использование. Договор о предоставлении лицензии подвергается государственной регистрации в Федеральной службе по интеллектуальной собственности, патентам и товарным знакам (Роспатент).
При этом, помимо собственно права на использование способа, лицензиат получает также многие необходимые сопутствующие сведения («ноу-хау»), а также методики, оборудование и реактивы для контроля режима обработки воды. Все это служит гарантией положительного результата в процессе водоподготовки. Немаловажным фактором успеха является и возможность получения личной консультации автора, а в необходимых случаях — и участие автора в наладке водно-химического режима.
Использование способа предотвращения солеотложений путем введения в воду фосфоновых кислот или их производных в случае, если выполняются условия (5–7), без зарегистрированного в установленном порядке разрешения патентообладателя, является нарушением патента и влечет за собой гражданско-правовую (материальную) ответственность, а также административную ответственность по ст. 7.12 Кодекса об административных правонарушениях РФ или уголовную ответственность по ст. 147 Уголовного Кодекса РФ вплоть до лишения свободы на срок до пяти лет.
Автор приглашает всех, кто заинтересован в легальном и эффективном использовании запатентованного способа ингибирования солеотложений, к взаимовыгодному сотрудничеству по внедрению описанного способа, а также организации необходимого химико-лабораторного контроля, обеспечивающего успешное предотвращение солеотложений.
Адсорбция — прилипание атомов, молекул или ионов к поверхности.
Ион — заряженный атом или молекула.
Ингибирование — торможение, замедление или полное предотвращение.
Лицензия — официальное разрешение на использование изобретения.
Моль — единица, применяемая для счета атомов, молекул или ионов, равная 6,02•1023.
Патент — официальный документ, удостоверяющий мировую новизну, изобретательский уровень и промышленную применимость изобретения, а также авторство и приоритет (первенство) изобретателя.
Флуктуация — случайное отклонение от равновесия, вызванное тепловым движением частиц.

























