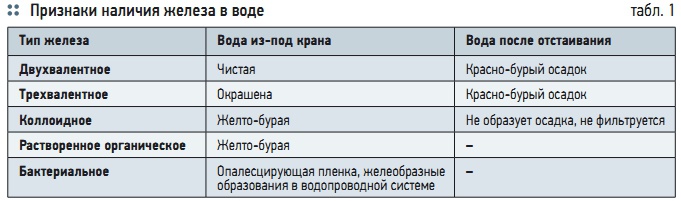
Табл. 1. Признаки наличия железа в воде
С водой, содержащей железо, возникает целый ряд проблем как при бытовом, так и при коммерческо-промышленном использовании. Уже при концентрациях железа свыше 0,3 мг/л такой водой образуются ржавые потеки, способные изменить цвет тканей при их стирке и т.п. При больших концентрациях у воды возникает характерный металлический привкус, что отрицательно сказывается на качестве напитков.
В некоторых случаях может пострадать даже качество еды, приготовленной на воде с высоким содержанием железа. Все это делает задачу по очистке воды от железа очень актуальной как для питьевого и хозяйственно-бытового применения, так и для промышленного использования. Железо существует в природе в различных формах (в зависимости от валентности): Fe, Fe+2, Fe+3, а также в виде различных сложных химических соединений.
- Элементарное железо (Fe). Элементарное, или металлическое железо, безусловно, нерастворимо в воде. В присутствии влаги и кислорода воздуха окисляется до трехвалентного, образуя нерастворимый оксид Fe2O3 (процесс, известный в быту как «ржавление»).
- Двухвалентное железо (Fe+2). Почти всегда находится в воде в растворенном состоянии, хотя возможны случаи (при определенных редко встречающихся в природной воде уровнях рН), когда гидроксид железа Fe(OH)2 способен выпадать в осадок.
- Трехвалентное железо (Fe+3). Гидроксид железа Fe(OH)3 нерастворим в воде (кроме случая очень низкого рН). Хлорид FeCl3 и сульфат Fe2(SO4) трехвалентного железа растворимы и могут образовываться даже в слабощелочных водах.
- Органическое железо. Органическое железо встречается в воде в разных формах и в составе различных комплексов. Органические соединения железа, как правило, растворимы или имеют коллоидную структуру и очень трудно поддаются удалению.
Различают виды органического железа:
- Бактериальное железо. Некоторые виды бактерий способны использовать энергию растворенного железа в процессе своей жизнедеятельности. При этом происходит преобразование двухвалентного железа в трехвалентное, которое сохраняется в желеобразной оболочке вокруг бактерии.
- Коллоидное железо. Коллоиды — это нерастворимые частицы очень малого размера (менее одного микрона), в силу чего они трудно поддаются фильтрации на гранулированных фильтрующих материалах. Крупные органические молекулы (такие, как танины и лигнины) также попадают в эту категорию. Коллоидные частицы из-за своего малого размера и высокого поверхностного заряда (отталкивающего частицы друг от друга, препятствуя их укрупнению) создают в воде суспензии и не осаждаются, находясь во взвешенном состоянии.
- Растворимое органическое железо. Так же как, например, полифосфаты, способны связывать и удерживать в растворе кальций и другие металлы, некоторые органические молекулы способны связывать железо в сложные растворимые комплексы, называемые хелатами. Примером такого связывания может служить удерживающая железо порфириновая группа гемоглобина крови или удерживающий магний хлорофилл растений. Так, прекрасным хелатообразующим агентом является гуминовая кислота, играющая важную роль в почвенном ионообмене. Все вышеперечисленные виды железа «ведут» себя в воде по-разному. Основные отличительные признаки приведены в табл. 1.
Необходимо только отметить, что «беда никогда не ходит одна» и на практике почти всегда встречается сочетание нескольких или даже всех видов железа. Учитывая, что нет единых утвержденных методик определения органического, коллоидного и бактериального железа, то в деле подбора эффективного метода (скорее, комплекса методов) очистки воды от железа очень много зависит от практического опыта специалиста, занимающегося водоочисткой.
Удаление из воды железа — без преувеличения одна из самых сложных задач в водоочистке. Даже беглый обзор существующих способов борьбы с железом позволяет сделать обоснованный вывод о том, что на данный момент не существует универсального экономически оправданного метода, применимого во всех случаях жизни. Каждый из существующих методов применим только в определенных пределах и имеет как достоинства, так и существенные недостатки. Итак, к существующим методам удаления железа можно отнести:
1. Окисление (кислородом воздуха или аэрацией, хлором, перманганатом калия, перекисью водорода, озоном) с последующим осаждением (с коагуляцией или без нее) и фильтрацией. Традиционный метод, применяемый уже много десятилетий. Так как реакция окисления железа требует довольно длительного времени, то использование для окисления только воздуха требует больших резервуаров, в которых можно обеспечить нужное время контакта.
Это наиболее старый способ и используется только на крупных муниципальных системах. Добавление же специальных окислителей ускоряет процесс. Наиболее широко применяется хлорирование, так как параллельно позволяет решать проблему с дезинфекцией. Наиболее передовым и сильным окислителем на сегодняшний день является озон. Однако установки для его производства довольно сложны, дороги и требуют значительных затрат электроэнергии, что ограничивает его применение.
Необходимо отметить также, что в концентрированном виде (например, на точке ввода в воду) озон является ядом (как, собственно говоря, и многие другие окислители) и требует очень внимательного к себе отношения. Частицы окисленного железа имеют достаточно малый размер (1–3 мкм) и поэтому осаждаются достаточно долго, поэтому применяют специальные химические вещества-коагулянты, способствующие укрупнению частиц и их ускоренному осаждению.
Применение коагулянтов необходимо также потому, что фильтрация на муниципальных очистных сооружениях осуществляется в основном на устаревших песчаных или антрацитовых осветлительных фильтрах (не способных задерживать мелкие частицы). Однако даже применение более современных фильтрующих засыпок (например, алюмосиликатов) не позволяет фильтровать частицы размером менее 20 мк. Проблему могло бы решить применение специальной керамики, но она достаточно дорого стоит (так как не производится в России).
У всех перечисленных способов окисления есть ряд недостатков. Во-первых, если не применять коагулянты, то процесс осаждения окисленного железа занимает долгое время, в противном же случае фильтрация некоагулированных частиц сильно затрудняется из-за их малого размера. Во-вторых, эти методы окисления (в меньшей степени это относится к озону) слабо помогают в борьбе с органическим железом. В-третьих, наличие в воде железа часто (практически всегда) сопровождается наличием марганца.
Марганец окисляется гораздо труднее, чем железо, и, кроме того, при значительно более высоких уровнях рН. Все вышеперечисленные недостатки сделали невозможным применение этого метода в сравнительно небольших бытовых и коммерческо-промышленных системах, работающих на больших скоростях.
2. Каталитическое окисление с последующей фильтрацией — наиболее распространенный на сегодняшний день метод удаления железа, применяемый в высокопроизводительных компактных системах. Суть метода заключается в том, что реакция окисления железа происходит на поверхности гранул специальной фильтрующей среды, обладающей свойствами катализатора (ускорителя химической реакции окисления). Наибольшее распространение в современной водоподготовке нашли фильтрующие среды на основе диоксида марганца MnO2: Birm, Greensand, Filox, Pyrolox и др.
Эти фильтрующие «засыпки» отличаются между собой как своими физическими характеристиками, так и содержанием диоксида марганца, и поэтому эффективно работают в разных диапазонах значений параметров, характеризующих воду. Однако принцип их работы одинаков. Железо (и в меньшей степени марганец) в присутствии диоксида марганца быстро окисляется и оседает на поверхности гранул фильтрующей среды. Впоследствии большая часть окисленного железа вымывается в дренаж при обратной промывке.
Таким образом, слой гранулированного катализатора является одновременно и фильтрующей средой. Для улучшения процесса окисления в воду могут добавляться дополнительные химические окислители. Наиболее распространенным является перманганат калия KMnO4 («марганцовка»), т.к. его применение не только активизирует реакцию окисления, но и компенсирует «вымывание» марганца с поверхности гранул фильтрующей среды, т.е. регенерирует ее. Используют как периодическую, так и непрерывную регенерацию.
Все системы на основе каталитического окисления с помощью диоксида марганца кроме специфических (не все из них работают по марганцу, почти все они имеют большой удельный вес и требуют больших расходов воды при обратной промывке) имеют и ряд общих недостатков. Во-первых, они неэффективны в отношении органического железа. Более того, при наличии в воде любой из форм органического железа на поверхности гранул фильтрующего материала со временем образуется органическая пленка, изолирующая катализатор — диоксид марганца от воды.
Таким образом, вся каталитическая способность фильтрующей засыпки сводится к нулю. Практически «на нет» сводится и способность фильтрующей среды удалять железо, т.к. в фильтрах этого типа просто не хватает времени для естественного протекания реакции окисления. Во-вторых, системы этого типа все равно не могут справиться со случаями, когда содержание железа в воде превышает 10–15 мг/л, что совсем не редкость. Присутствие в воде марганца только усугубляет ситуацию.
3. Ионный обмен как метод обработки воды известен довольно давно и применялся (да и теперь применяется) в основном для умягчения воды. Раньше для реализации этого метода использовались природные иониты (сульфоугли, цеолиты). Однако с появлением синтетических ионообменных смол эффективность использования ионного обмена для целей водоочистки резко возросла.
С точки зрения удаления из воды железа важен тот факт, что катиониты способны удалять из воды не только ионы кальция и магния, но и другие двухвалентные металлы, а значит и растворенное двухвалентное железо. Теоретически, концентрации железа, с которыми могут справиться ионообменные смолы, очень велики. Достоинством ионного обмена является также и то, что он «не боится» верного спутника железа — марганца, сильно осложняющего работу систем, основанных на использовании методов окисления.
Главное же преимущество ионного обмена то, что из воды могут быть удалены железо и марганец, находящиеся в растворенном состоянии. То есть, в процессе обработки совсем отпадает необходимость в такой капризной и «грязной» (из-за необходимости вымывать ржавчину) стадии как окисление.
























