Первое, что приходит в голову, когда смотришь на график фиксируемых параметров работы установки Na-катионирования воды (например, рис. 5), — это «электрокардиограмма» данного устройства. Мы как бы видим «ритм его сердца». Пока «сердце» бьётся — установка «жива». Как только перепады прекращаются — установка «умирает», то есть перестаёт умягчать воду. Но обо всём по порядку…
Известно, что электропроводность воды зависит от количества растворённого в воде вещества (ионов). Электропроводность подавляющего большинства природных вод обеспечивается шестью видами ионов: катионы — кальций (Ca), магний (Mg), натрий + калий (далее — натрий Na); анионы — бикарбонат (HCO3), сульфаты (SO4); хлориды (Cl). Перенос заряда в воде осуществляется ионами. Подробно процесс переноса электрического заряда в воде рассмотрен в статье [1]. Если рассматривать электропроводность воды с ионами жёсткости (Ca, Mg) и электропроводность той же самой, но умягчённой воды, то есть воды только с катионами натрия, то её электропроводность почти всегда будет выше, чем исходной жёсткой. Это происходит не из-за того, что молярная масса натрия немного больше, чем кальция и магния при эквивалентном замещении (Na = 23×2 = 46 против Cа = 40, Mg = 24), и, соответственно, солесодержание умягчённой воды возрастает, а вследствие того, что одновалентный натрий теряет меньше подвижности в среде других ионов, чем двухвалентные ионы кальция и магния, и может перенести больше электрического заряда, чем двухвалентные кальций и магний.
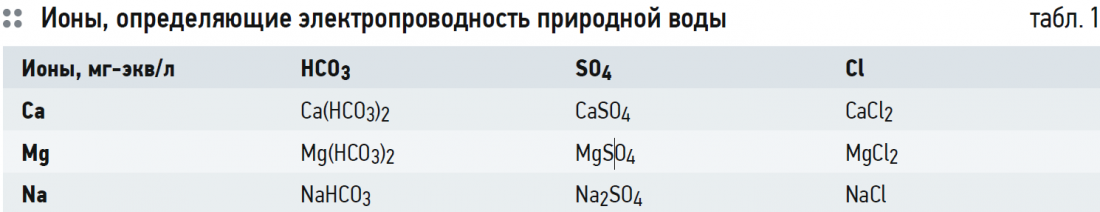
Значение электропроводности отдельного иона не имеет физического смысла, так как в воде ион удерживает вокруг себя ионную оболочку из противоположно заряженных ионов и, соответственно, испытывает тормозящее воздействие со стороны ионов противоположного заряда. Можно достаточно точно определить значение электропроводности воды только для конкретной соли, а также определить уменьшение подвижности (эквивалентной электропроводимости) при увеличении концентрации данной соли. Ионы, определяющие электропроводность природной воды, представлены в табл. 1. Как видно из данной таблицы, в воде шестью типами ионов может быть образовано девять солей (шесть солей сильных кислот — сульфат и хлорид; три соли слабой кислоты — бикарбонат-угольной).
С точки зрения взаимного влияния ионов можно сказать, что в воде содержатся три типа солей следующих валентностей:
- 1:1 (NaHCO3, NaCl и т. п.);
- 2:1 (Ca(HCO3)2, Mg(HCO3)2, CaCl2, MgCl2, Na2SO4 и т. п.);
- 2:2 (CaSO4, MgSO4 и т. п.).
Если воду данного состава умягчить при помощи пропускания через катионит в Na-форме, то полученная жидкость будет содержать в качестве катионов только ионы Na, то есть только соли 1:1 (NaHCO3, NaCl) и 2:1 (Na2SO4).
Потеря подвижностей ионов солей 1:1 и 2:1 в области низких концентраций (до 10 ммоль/л) практически одинакова. То есть, если в исходной воде содержатся только соли 1:1 и 2:1, то после замещения в такой воде всех катионов на катионы Na значение её электропроводности станет меньше или останется такой же. В этом случае в исходной воде не содержится сульфат, и в умягчённой будут содержаться только соли 1:1.
Если в исходной воде содержится сульфат, то это значит, что в ней имеется соль 2:2 и после умягчения она становится сульфатом натрия, то есть солью 2:1. Соответственно, в этом случае падение подвижности соли 2:1 значительно меньше, чем падение 2:2. Поэтому электропроводность такой воды будет больше электропроводности жёсткой. При этом, чем больше концентрация солей в исходной воде, тем выше электропроводность умягчённой по отношению к исходной.
Отсюда следует следующий вывод. Чем больше в исходной воде содержится сульфат-иона, тем больше разница между значением электропроводности умягчённой воды по отношению к электропроводности исходной, и тем качественнее можно осуществлять кондуктометрический контроль за работой установок Na-катионирования воды.
Тем не менее, при жёсткости исходной воды более 8 мг-экв/л, даже при отсутствии в воде сульфата электропроводность умягчённой будет больше электропроводности исходной. Хотя перепад в данном случае будет и незначительным, это значительно затрудняет качественный контроль процесса Na-катионирования такой воды с использованием электропроводности.
Можно с достаточной точностью определить значение электропроводности раствора в зависимости от его концентрации для каждой конкретной соли. Но, как видно, из табл. 1 в воде существует минимум девять солей, определяющих её электропроводность.
Для того, чтобы определить концентрацию каждой соли в воде, необходимо сделать предположение, что ионная оболочка каждого иона равномерно распределена, то есть соотношение различных ионов в любой момент времени в любой части объёма воды одинаково. Фактически должно наблюдаться равномерное распределение ионов в объёме воды, взятых в мг-экв/л.
Соответственно, можно определить долю каждой соли и, зная концентрацию каждого иона (из химических анализов), возможно выяснить концентрацию каждой из солей путём умножения концентрации каждого иона на долю каждой (соответствующей) соли.
Зная концентрацию каждой соли, можно определить значение электропроводности любой из них. Затем, по аналогии, используя подход чисел переноса в определении электропроводности отдельного иона, можно определить значение электропроводности воды, содержащей все соли, представленные в табл. 1.
На основании описанного подхода автором была разработана программа расчёта значения электропроводности воды в зависимости от её ионного состава. В результате работы над данной программой выяснилась принципиальная возможность контроля процесса Na-катионирования воды по значению электропроводности. Более того, при помощи указанного программного обеспечения можно определить ионный состав воды. Для этого необходимо знать электропроводности исходной и умягчённой воды, а также её жёсткость и щёлочность.
Например, произведём расчёт электропроводности исходной воды по известному ионному составу.
Катионы
Исходная вода
- Сa — 0,001 моль/л (0,002 мг-экв/л);
- Mg — 0,0006 моль/л (0,0012 мг-экв/л);
- Na — 0,0009 моль/л (0,0009 мг-экв/л).
Умягчённая вода
- Na — 0,0041 моль/л (0,0041 мг-экв/л);
- Сумма К — 0,0041 мг-экв/л.
Анионы:
- HCO3–0,002 моль/л (0,002 мг-экв/л);
- SO4–0,0007 моль/л (0,0014 мг-экв/л);
- Cl — 0,0007 моль/л (0,0007 мг-экв/л);
- Сумма А — 0,0041 мг-экв/л;
- Сумма К равна сумме А.
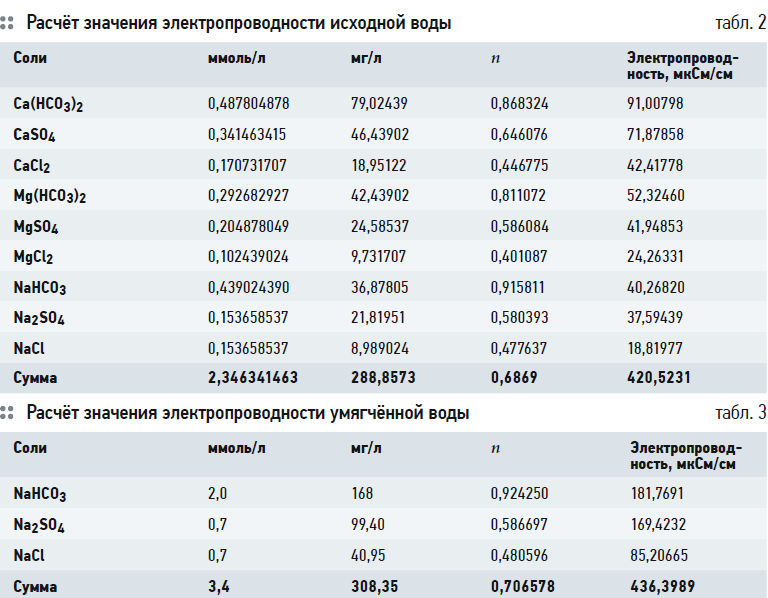
Результаты расчёта представлены в табл. 2. В табл. 3 представлен результат расчёта значения электропроводности для полностью умягчённой воды. В качестве катионов в такой воде присутствуют только катионы натрия, поэтому расчёт ведётся только для трёх солей. Разница между электропроводностью умягчённой и исходной воды: 436–420 = 16 мкСм/см.
Затем пропорционально увеличим значение жёсткости умягчённой воды, эквивалентно уменьшая значение натрия. Возьмём шесть значений:
- Са = 0,0001; Mg = 0,00005; Na = 0,004 моль/л (жёсткость — 0,3 мг-экв/л);
- Са = 0,0002; Mg = 0,0001; Na = 0,0037 моль/л (жёсткость — 0,6 мг-экв/л);
- Са = 0,0004; Mg = 0,0002; Na = 0,0031 моль/л (жёсткость — 1,2 мг-экв/л);
- Са = 0,0006; Mg = 0,0003; Na = 0,0025 моль/л (жёсткость — 1,8 мг-экв/л);
- Са = 0,0008; Mg = 0,0004; Na = 0,0019 моль/л (жёсткость — 2,4 мг-экв/л);
- Са = 0,0001; Mg = 0,0005; Na = 0,0013 моль/л (жёсткость — 3,0 мг-экв/л).
При каждом значении кальция, магния и натрия при помощи программы определим электропроводность. Результаты расчёта представлены на рис. 1. Как можно видеть, зависимость носит линейный характер. Это известное условие, к примеру, используется в патенте (Dopslaff Hartmut; Dopslaff Carsten H+ «Blending control method with determination of untreated water hardness via the conductivity of the soft water and blended water», Application number Z2013072056220131217).
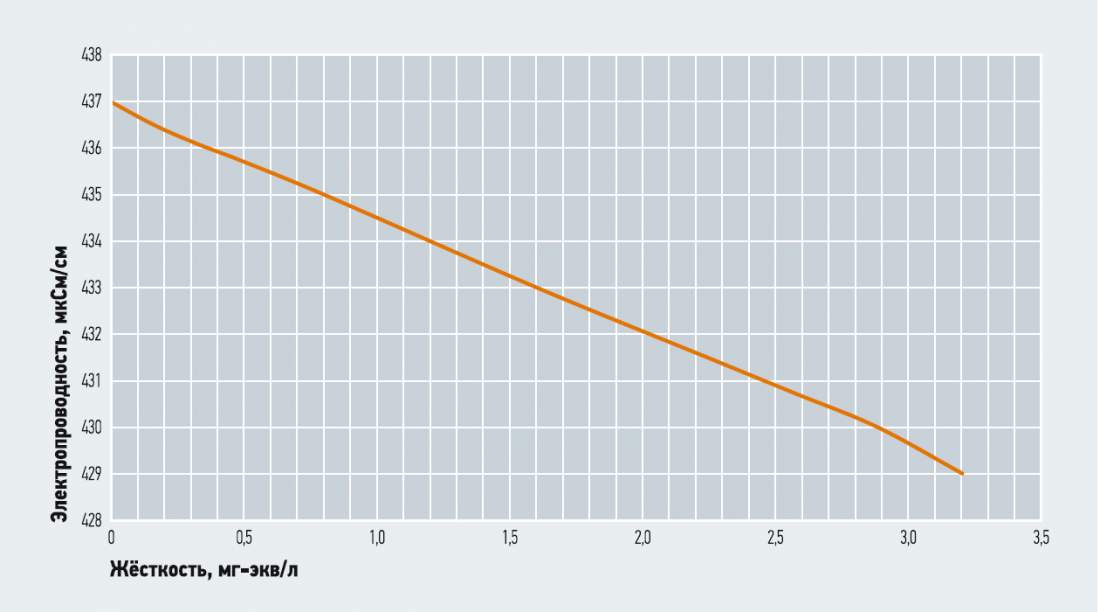
Рис. 1. Зависимость электропроводности воды от жёсткости
Известно, что фильтроцикл установок умягчения рассчитывается исходя из жёсткости умягчённой воды 0,1 мг-экв/л. При этом установка умягчения выводится в регенерацию поваренной солью при значении жёсткости умягчённой воды не более 0,5 мг-экв/л. Соответственно, если электропроводность умягчённой жидкости имеет значение 434–433 мкСм/см, то можно считать, что вода данного ионного состава содержит остаточную жёсткость не более 0,1 мг-экв/л.
Для проверки данного предположения удобно использовать схему с дистанционным контролем значения измеренной электропроводности. Для этого решено было использовать оборудование компании ОВЕН. В схеме задействован «облачный» сервис, куда передаются данные об измеренной электропроводности умягчённой воды и имеется возможность отслеживать значения электропроводности в виде графика от времени, что крайне удобно для подобных задач.
Для измерения электропроводности был приобретён датчик электропроводности с трансмиттером с выходным сигналом 4–20 мА. Для передачи значений электропроводности, измеренных датчиком, фирма ОВЕН предоставила набор оборудования в составе программируемого реле ПР-100, сетевого шлюза ПМ-210 GPRS и блока питания БП-30А 24 В.
Данное программируемое реле используется для получения значения электропроводности умягчённой воды по аналоговому входу 4–20 мА от датчика электропроводности. Затем, при помощи сетевого шлюза ПМ-210, подключённого по интерфейсу RS-485, значение передаётся в OwenCloud. На сервисе значения электропроводности умягчённой воды визуализируются в виде графика зависимости от времени измерения.
Используя данную схему контроля, был проведён следующий эксперимент.
Производилось умягчение воды в ионообменной колонке. Жёсткость исходной воды — 2,8 мг-экв/л. Объём катионита в колонке — 0,55 л. Расход воды через колонку — 50 л/ч. Линейная скорость фильтрования — 32 м/ч. Расчётный фильтроцикл — 220–240 л.
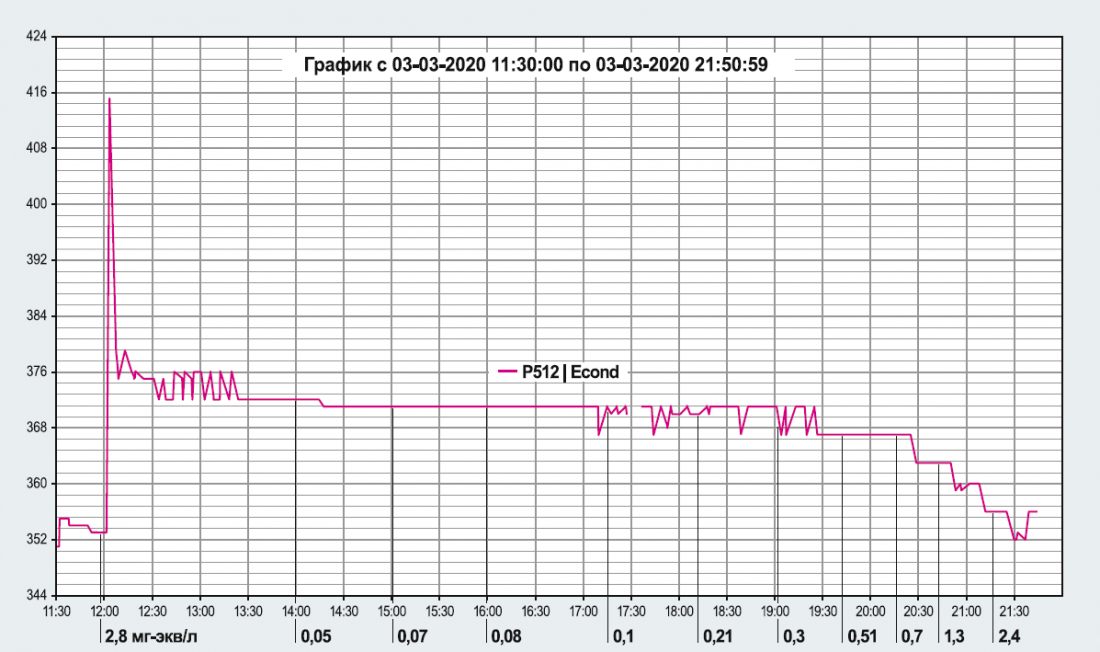
Рис. 2. Данные мониторинга работы колонки умягчения воды при помощи сервиса OwenCloud
На рис. 2 представлены данные мониторинга при помощи сервиса OwenCloud работы колонки умягчения воды от момента регенерации до момента полного истощения катионита по ионам натрия. Из данного рисунка следует, что колонка начала умягчать воду после регенерации в 12:00. Видно, что электропроводность умягчённой воды несколько повышена за счёт остаточных солей после отмывки от регенерационного раствора. Затем электропроводность держится практически на постоянном уровне.
В 12:00, фактически в самом начале фильтроцикла, значение электропроводности составило 376 мкСм/см. При этом анализ воды на жёсткость показал значение 0,04 мг-экв/л. В течение 5,5 ч электропроводность воды оставалась на уровне 374 мкСм/см, а жёсткость не превышала 0,1 мг-экв/л. Через 5,5 ч работы установки умягчения жёсткость умягчённой воды составила 0,12 мг-экв/л и электропроводность была на уровне 372 мкСм/см. Объём умягчённой воды к этому времени составил 175 л.
Затем в течение часа произошло уменьшение значения электропроводности до 371 мкСм/см, а жёсткость при этом была равной 0,3 мг-экв/л. Затем, ещё через полчаса, электропроводность упала до 367 мкСм/см, а жёсткость выросла до 0,5 мг-экв/л. Через 7 ч работы электропроводность начала быстро падать и через 8,5–9 ч достигла значения электропроводности исходной жёсткой воды.
Используя полученные данные, можно построить зависимость, на которой будет наглядно видно, какой объём обменной ёмкости катионита обеспечивает фильтроцикл, а какой — качество умягчённой воды, полученной в объёме этого фильтроцикла.
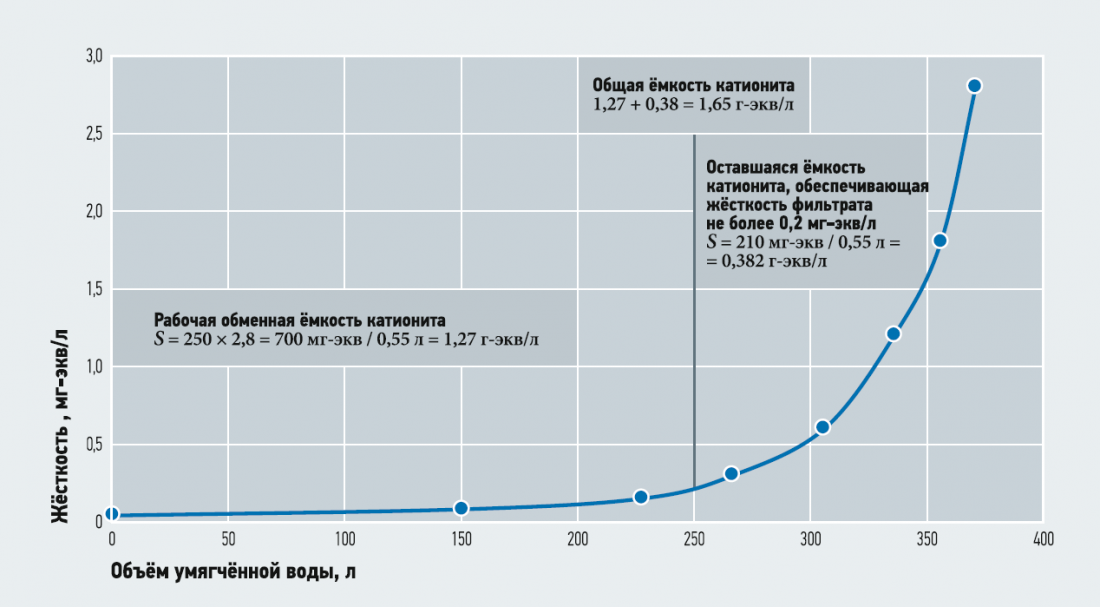
Рис. 3. Зависимость жёсткости умягчённой воды от объёма обработанной воды
На рис. 3 изображена зависимость жёсткости умягчённой воды от объёма воды, прошедшей установку умягчения. Как видно из рис. 3, жёсткость умягчённой воды не более 0,1 мг-экв/л обеспечивалась в объёме фильтроцикла 180 л. При этом жёсткость умягчённой жидкости, равная 0,2 мг-экв/л, обеспечивалась в объёме 250 л. Только после прохождения 300 л умягчаемой воды жёсткость фильтрата составила чуть больше 0,5 мг-экв/л. Рекомендуемый фильтроцикл для данного количество катионита составил 240 л. Жёсткость воды при этом не превышала 0,2 мг-экв/л.
Как мы можем видеть, резкое увеличение жёсткости фильтрата происходит после того, как этот его параметр дойдёт до 0,5 мг-экв/л. Поэтому при работе установки умягчения в качестве первой ступени рекомендуется выводить установку в регенерацию при жёсткости фильтрата 0,5 мг-экв/л, а расчёт фильтроцикла вести для жёсткости фильтрата 0,1 мг-экв/л.
На рис. 2 показано, что резкое уменьшение электропроводности происходило после достижения фильтратом жёсткости 0,3 мг-экв/л. Соответственно, зная перепад значений электропроводности между умягчённой и исходной водой и отслеживая уровень падения электропроводности умягчённой воды можно достаточно чётко отследить уровень жёсткости получающегося фильтрата установки умягчения.
Необходимо уточнить ещё один очень важный момент. Построим график зависимости между электропроводностью фильтрата установки умягчения и его жёсткостью полученными в вышеописанном эксперименте. График зависимости представлен на рис. 4. Эта кривая аналогична представленной на рис. 1. Только график на рис. 1 использует расчётные данные. Сразу очевидно отличие.
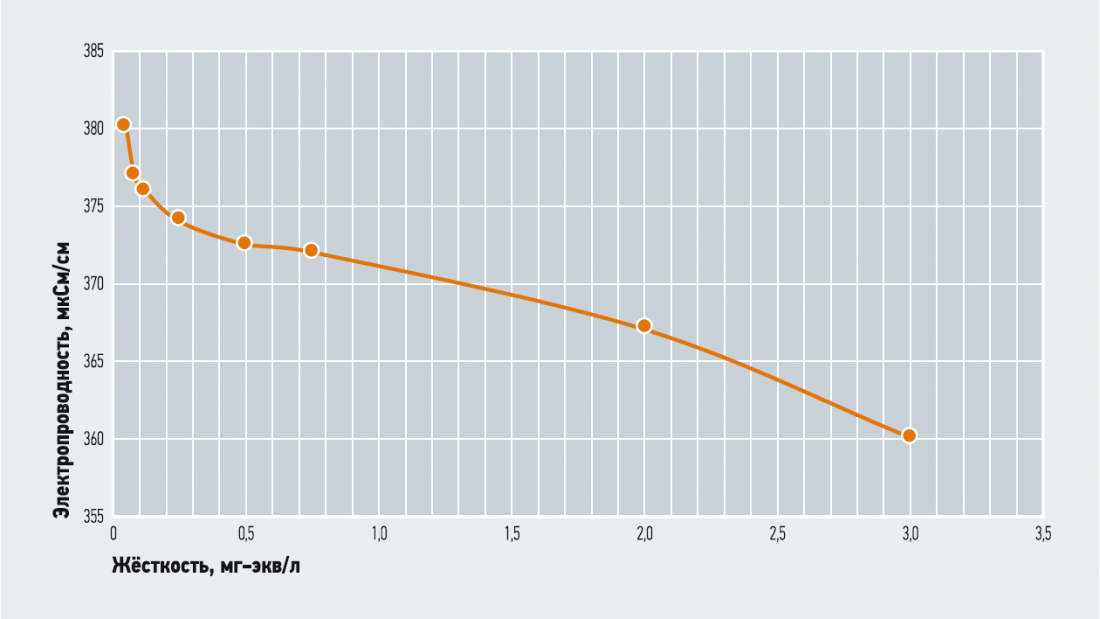
Рис. 4. Зависимость между электропроводностью фильтрата установки и его жёсткостью
График на рис. 4 имеет линейный характер только в интервале жёсткости от 0,5 до 3,0 мг-экв/л. В интервале от 0 до 0,5 наблюдается резкое уменьшение значения электропроводности воды. Для уточнения этого обстоятельства было проведено несколько экспериментов и все они подтвердили данную зависимость. Вероятно, данное «особенное» поведение электропроводности в области небольших значений концентраций ионов жёсткости фильтрата определяется тем, что ионы кальция и магния при концентрациях менее 0,1 мг-экв/л образуют ионные пары с сульфатом и, соответственно, не переносят электрический заряд.
При увеличении концентрации ионов жёсткости в фильтрате более 0,1 мг-экв/л начинается их равномерное распределение по ионным оболочкам и уменьшение значения электропроводности при увеличении жёсткости фильтрата носит линейный характер, так как кальций и магний равномерно встраиваются в ионные оболочки хлоридов, бикарбонатов и сульфатов, находящихся в воде.
В любом случае это обстоятельство необходимо учитывать при организации процесса контроля работы установки умягчения при помощи значения электропроводности воды. Иначе фильтроцикл этого устройства может быть определён как значительно меньший, чем на самом деле со всеми вытекающими последствиями (перерасход соли, повышенное количество сточных вод и т. п.).
Данная технология контроля была внедрена на Саратовском молочном комбинате. Скриншоты фиксируемых параметров работы установки Na-катионирования воды в паровой котельной Саратовского молочного комбината представлены на рис. 5.
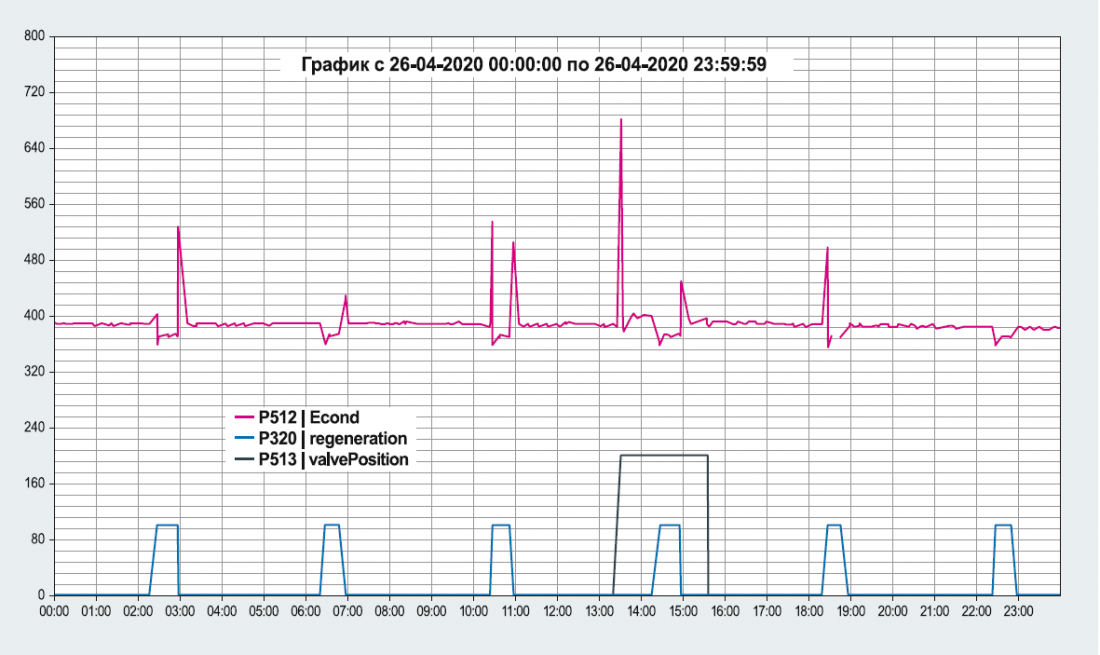
Рис. 5. Фиксируемые параметры работы установки Na-катионирования воды в паровой котельной Саратовского молочного комбината
Измерение значения электропроводности воды производилось одним и тем же датчиком. При этом каждые 3,5 ч производилось измерение электропроводности исходной воды в течение 30 мин. Всё остальное время измерялась электропроводность уже умягчённой. За счёт этого появились характерные перепады в измерении значений электропроводности похожие на сердечный ритм.
Использование одного датчика электропроводности позволяет избежать ошибки в измерениях и чётко контролировать перепад между электропроводностью умягчённой и исходной воды. На это решение подана заявка на патент.
На рис. 5 можно видеть, что постоянно происходит мониторинг электропроводности воды. При этом при пике (100) происходит измерение электропроводности исходной в течение 30 мин. Всё остальное время (3,5 ч) тестируется умягчённая вода. Пик (200) показывает, что осуществляется регенерация одного из фильтров установки умягчения Twin. Можно проследить, что этот процесс продолжается два часа. Также есть возможность наблюдать, как изменяется значение электропроводности между исходной и умягчённой водой.
В данном случае значение параметра исходной воды — 353 мкСм/см, а умягчённой — 368 мкСм/см. Перепад, равный 15 мкСм/см, говорит о том, что установка умягчения даёт именно умягчённую воду, то есть работает в пределах установленного фильтроцикла.
После установки данной системы контроля на предприятии в течении трёх дней был определён оптимальный фильтроцикл работы установки умягчения. Он составил 35 м³. При этом расчётный фильтроцикл, введённый ранее в автоматический клапан управления установки умягчения, составлял 25 м³. Фильтроцикл был увеличен более, чем на 30%. Также была выявлена внутренняя протечка клапана управления одного фильтра умягчения, работающего по системе Twin. Из-за этого один фильтр постоянно давал небольшую повышенную жёсткость, что было достаточно проблематично выявить в условиях того, что я производил только один анализ воды на жёсткость в месяц.
В настоящее время ведётся постоянный удалённый мониторинг работы системы умягчения, что в условиях пандемии коронавируса оказалось эффективным и безопасным способом контроля.
Подводя итог, хочу сказать, что контроль процесса умягчения воды по электропроводности вполне возможен и значительно увеличивает эффективность работы установки умягчения без проведения постоянных химических анализов воды на жёсткость. Более того, контроль по электропроводности при соответствующей грамотной организации процесса более эффективен, чем проведение периодических химических анализов, так как электропроводность измеряется постоянно и сразу реагирует на изменение жёсткости фильтрата. При этом данный контроль позволяет чрезвычайно просто определить оптимальный фильтроцикл работы установки умягчения, значительно упрощает и повышает качество проведения пусконаладочных работ на установках умягчения.
Жёсткость исходной воды поверхностных источников меняется в зависимости от времени года. К примеру, жёсткость воды в реке Волге меняется от 2,8 до 4,8 мг-экв/л (как правило, от 3,0 до 4,2). Соответственно, фильтроцикл установок умягчения, работающих на такой воде, будет меняться до 30%. Зная это обстоятельство, современные автоматические установки умягчения настраиваются на самое высокое значение жёсткости. При этом в летне-осенний период (при минимальной жёсткости) фильтроцикл мог бы быть увеличен на 20–30%. Контроль по электропроводности позволяет легко это отслеживать, и даже неспециалист сможет настроить оптимальный фильтроцикл в зависимости от текущего значения жёсткости исходной воды.
Резюме
Способ измерения электропроводности воды для контроля установок умягчения носит важный, во многом определяющий работу системы характер. На этом способе измерения электропроводности воды автором получен патент [2]. В настоящее время установка контроля системы умягчения воды уже эксплуатируется на промышленном предприятии.
























