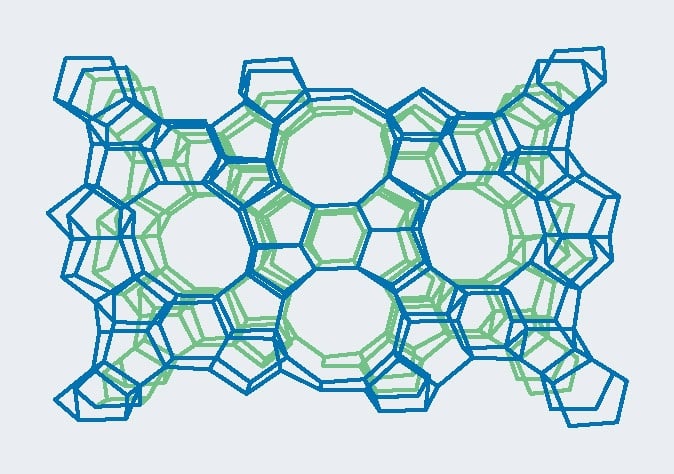
Рис. 1. Трёхмерная кристаллическая структура природного минерала цеолита типа ZSM-5
В статье приведены данные о наноструктуре, полученные с помощью сканирующей электронной микроскопии (СЭМ), газовой хроматографией и инфракрасной-спектроскопией (НЭС- и ДНЭС-методы). Измерены cредние энергии (ΔEH-O) водородных Н-О-связей между молекулами H2O в образцах воды после её обработки шунгитом и цеолитом, составляющие +0,0025 ± 0,0011 эВ для шунгита, и -1,2 ± 0,0011 эВ для цеолита, соответственно. Полученные данные могут быть использованы для создания фильтров воды на основе шунгита и цеолита.
Введение
Шунгит (посёлок Шуньга, Карелия, Россия) и цеолит (местечко Мост, Болгария) относятся к новому поколению природных минеральных сорбентов (ПМС). Шунгит — промежуточный продукт между аморфным углеродом и кристаллическим графитом, содержащий углерод (30 масс. %), кварц (45 масс. %) и силикатные слюды (около 20 масс. %).
Цеолиты являются алюмосиликатными минералами натрия, калия или других элементов. Природные цеолиты образуются в условиях высоких температур и давлений при контакте вулканических пород и слоёв пепла с щелочными грунтовыми водами.
В качестве ПМС шунгит и цеолит широко применяются в химической промышленности и индустрии. Шунгит используется в качестве наполнителя и заменителя кокса в доменном производстве высококремнистого чугуна, при выплавке ферросплавов, в производстве термоустойчивых красок и антипригарных покрытий и как наполнитель резины.
Шунгитовые породы обладают сорбционными, бактерицидными, каталитическими, восстановительными свойствами, а также способностью экранировать электромагнитные и радиоизлучения [1]. Эти свойства позволили использовать шунгит для создания различных материалов с наномолекулярной структурой. На основе шунгита созданы электропроводные краски, наполнители полимерных материалов и резин, заменители сажи и технического углерода бетоны, кирпичи, штукатурные растворы, асфальты, а также экранирующие электромагнитное и радиоизлучение композиционные материалы.
Сорбционные, каталитические и восстановительные свойства шунгита способствовали его использованию в водоподготовке для очистки сточных вод от неорганических и органических веществ (тяжёлые металлы, аммиак, нефтепродукты, пестициды, фенолы, поверхностно-активные вещества и др.) [2].
Цеолиты являются алюмосиликатными минералами натрия, калия или других элементов. Природные цеолиты образуются в условиях высоких температур и давлений при контакте вулканических пород и слоёв пепла с щелочными грунтовыми водами
Кроме этого, шунгит является эффективным сорбентом для очистки воды от хлора и хлорорганических веществ (диоксинов, радикалов), обладает бактерицидными свойствами по отношению к патогенной микрофлоре в воде.
Цеолиты, благодаря их способности поглощать или пропускать через кристаллический каркас молекулы других химических соединений, могут использоваться как своеобразные молекулярные сита для разделения смеси газов и жидкостей [3]. Кроме этого, цеолиты являются ионообменниками катионного типа, способными извлекать из воды тяжёлые металлы, и, по сравнению с синтетическими смолами, обладают повышенной избирательностью к ионам цезия, свинца, кадмия и стронция. Эффективны цеолиты и в отношении органических соединений, например, концентрация наиболее распространённого в воде канцерогена бензапирена уменьшается при фильтровании через фильтр с цеолитом почти в 250 раз. Замена действующих фильтрующих материалов на цеолит позволяет повысить производительность водоочистных сооружений почти в два раза. Природные цеолиты используются в виде порошков и фильтрующих материалов для очистки воды от поверхностно-активных веществ (ПАВ), тяжёлых металлов, ароматических органических соединений, красителей, пестицидов, коллоидных и бактериальных загрязнений. После использования цеолит подвергается многократной регенерации исходной водой или солевым раствором, в зависимости от целевого использования.
Высокий спектр свойств шунгита и цеолита определяет поиск новых областей практического применения этих минералов, что способствует более глубокому изучению структуры шунгита и цеолита с помощью современных методов анализа. Целью настоящей работы являлось исследование структурных свойств шунгита и цеолита и построение математической модели взаимодействия этих минералов с водой.
Структурные свойства и состав шунгита и цеолита
Цеолит и шунгит относятся к новому поколению ПМС. Шунгит по структуре представляет собой аллотропную форму метастабильного углерода, находящегося на предграфитовой стадии углефикации [4]. В состав шунгита, кроме углерода, входят SiO2 (57,0 масс. %), TiO2 (0,2), Al2O3 (4,0), FeO (0,6), Fe2O3 (1,49), MgO (1,2), MnO (0,15), К2О (1,5) и S (1,2) (табл. 1). В продукте, полученном при термическом обжиге шунгита (шунгизит) при 1200-1400 °C, обнаруживаются в небольших количествах V (0,015 масс. %), B (0,004), Ni (0,0085), Mo (0,0031), Cu (0,0037), Zn (0,0067), Co (0,00014), As (0,00035), Cr (0,0072) и Zn (0,0076).
Цеолит — алюмосиликатный минерал, состоящий из алюмосиликатного каркаса с щёлочноземельными металлами натрия, калия или других элементов. Кристаллическая структура цеолитов образована тетраэдрами [AlO4]2- и [SiO4]2-, объединёнными общими вершинами, отрицательные заряды которых компенсируются катионами (H+, Na+, K+, Ca2+, NH+), в большинстве случаев способными в катионному обмену в водных растворах. В промежутках кристаллического каркаса расположены гидратированные положительные ионы щелочных и щёлочноземельных металлов — натрия, калия, кальция, реже магния, бария, стронция, компенсирующих заряд каркаса, и молекулы воды. Тетраэдры [AlO4]2- и [SiO4]2- образуют вторичные структурные единицы, такие как шестичленные кольца, пятичленные кольца, усечённые октаэдры и др. (рис. 1). Кристаллический каркас из алюмосиликатов включает взаимодействие каналов и полостей, образующих пористую структуру с формированием «молекулярных пор» размерами 0,3-1,0 нм. Размеры каналов достаточны для проникновения в них органических молекул и катионов, а суммарный объём их вместе с порами достигает 50 %. Средний размер кристаллической решётки цеолита может варьировать в диапазоне от 0,5 до 30 мкм.
Общая химическая формула цеолитов может быть представлена как:
Ме(2/n)[(Аl2O3)×(SiO2)y]⋅zН20, (1)
где Me — катион щелочного металла; n — его валентность; x и у — мольные соотношения оксидов кремния и алюминия в каркасе цеолита, указывающие на количество катионообменных позиций в структуре (у = 2 - ∞); z — количество молекул воды. Известно более 30 видов природных цеолитов, но лишь часть из них образует крупные месторождения (80 % концентратов), удобные для промышленной переработки. Наиболее распространены природные цеолиты:
- шабазит (Ca, Na2) — [Al2Si4O12]·6H2O с размерами ячейки 0,37-0,50 нм;
- морденит (Ca, Na2, K2), имеющий формулу [Al2Si10O24]·7H2O с размерами ячейки 0,67-0,70 нм;
- клинопптиломит (Na2, K2, Ca), имеющий формулу [Al2O310SiO2]·8H2O с размерами ячейки 0,75-0,82 нм.
Синтетические цеолиты имеют строение и кристаллическую структуру, аналогичные природным цеолитам:
- цеолиты типа А относятся к низкокремнистым формам: в них отношение SiO2:Al2O3 не превышает двух;
- цеолиты типа X имеют отношение SiO2:Al2O3, которое может изменяться от 2,2 до 3,3;
- цеолиты типа Y характеризуются соотношением SiO2:Al2O3 в пределах от 3,1 до 6 (причём при увеличении этого показателя повышается кислотостойкость цеолитов).
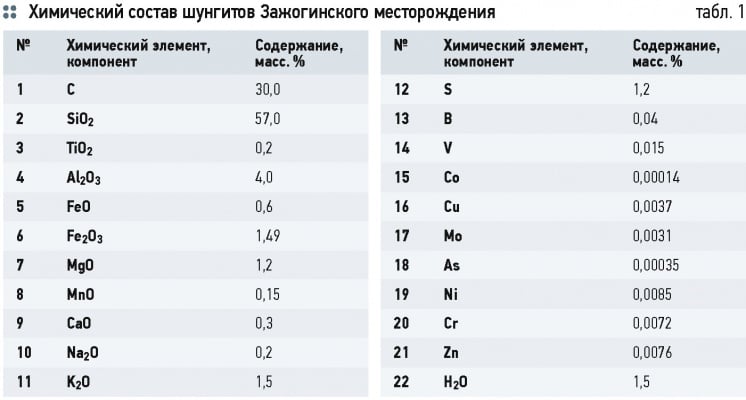
Размеры пор, определяющих избирательность цеолитов, находятся в пределах 0,0003 до 0,0009 мкм. Элементный состав анализируемого цеолита из болгарского местечка Мост аналогичен таковому для шунгита (табл. 2), за исключение углерода, который не встречается в цеолите и некоторых других элементов. Количества основных элементов (SiO2, TiO2, Al2O3, FeO, Fe2O3, MgO, CaO, Na2O, K2O, S), составляющие эти минералы отличаются от шунгита: ив цеолите их содержание выше, чем у шунгита, за исключением TiO2 и K2O, содержания которых в цеолите снижены (табл. 2).
Содержания микроэлементов — V (0,0272 %), Co (0,0045 %), Cu (0,0151 %), Mo (0,0012 %), As (0,0025 %), Ni (0,0079 %), Zn (0,1007 %), Zn (0,1007 %), Ba (0,0066 %) и Cr (0,0048 %) — увеличены в цеолите по сравнению с шунгитом (табл. 2).
Физико-химические свойства шунгита и цеолита достаточно хорошо изучены [5, 6]. Плотность шунгита составляет 2,1-2,4 г/см3; пористость — до 5 %; прочность на сжатие — 100-120 МПа; коэффициент электропроводности — 1500 См/м; коэффициент теплопроводности — 3,8 Вт/(м-К); адсорбционная ёмкость — 15-20 м2/г. Плотность цеолита — 1,7-2,1 г/см3; пористость — 51 % объёма каркаса; адсорбционная ёмкость 5 м2/г; средний размер пор — 4-6 А; твёрдость по шкале Мооса — 4-5.
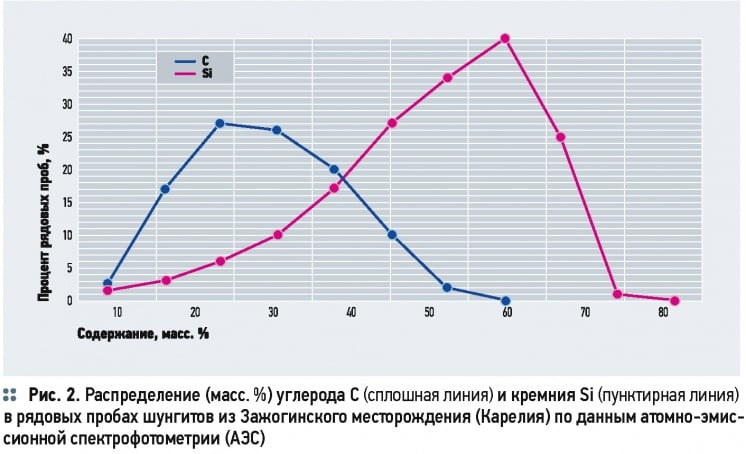
Шунгиты и цеолиты различаются по составу минеральной основы (алюмосиликатной, кремнистой), а шунгиты дополнительно — по количеству шунгитового углерода. Шунгиты с силикатной минеральной основой подразделяются на малоуглеродистые (до 5 масс. % С), среднеуглеродистые (5-25), а также высокоуглеродистые (25-80) [7]. Сумма (C + Si) в шунгитах Зажогинского месторождения находится в пределах 83-88 масс. % (рис. 2). Мольные соотношения оксидов кремния и алюминия в алюмо силикатном каркасе цеолита составляют 2-3 ед.
Исследования ультратонких шлифов шунгита методом просвечивающей (трансмиссионной) электронной микроскопии (ПЭМ) и растровой электронной микроскопии (РЭМ) в поглощённых и обратнорассеянных электронах [8] показали, что шунгитовый углерод равномерно распределён в силикатном каркасе из мелкодисперсных кристаллов кварца, размерами 1-10 мкм.
Углеродистое вещество шунгита является продуктом высокой степени карбонизации углеводородов. Его элементный состав: С — 98,6-99,6 масс. %; Н — 0,150,5; (Н + О) — 0,15-0,9. При практически постоянном элементном составе шунгитового углеродистого вещества наблюдается непостоянство его структур — молекулярной, надмолекулярной, поверхностной и пористой [9].
Основу шунгитного углерода составляют полые, многослойные фуллереноподобные сферические глобулы диаметром 10-30 нм, содержащие пакеты плавно изогнутых углеродных слоёв, охватывающих нанопоры.
Структура глобулы устойчива относительно фазовых переходов шунгитового углерода в другие аллотропные формы. Фуллереноподобные глобулы могут содержать от нескольких десятков до нескольких сотен атомов углерода и различаться по форме и размерам [10].
Углеродистое вещество шунгитов обладает структурной анизотропией и проявляет существенное увеличение диамагнетизма при пониженных температурах, характерное для кристаллов, образованных молекулами фуллеренов (фуллериты). Фуллериты являются молекулярными кристаллами с гранецентрированной кубической (ГЦК) решёткой размером 1,42 нм, числом ближайших соседей — 12 и расстоянием между ближайшими соседями — 1 нм. Плотность фуллерита составляет 1,7 г/см3, что несколько меньше плотности и шунгита (2,1-2,4 г/см3) и графита (2,3 г/см3). Молекулы фуллеренов могут содержать 24, 28, 32, 36, 50, 60, 70 и т.д. атомов углерода. Фуллерены с количеством углеродных атомов n < 60 являются неустойчивыми. Высшие фуллерены, содержащие большее число атомов углерода (n < 400), образуются в незначительных количествах и часто имеют довольно сложный изомерный состав [11]. В углеродистом веществе шунгитовых пород выявлены фуллерены (С60, С70, С74, С76, С84 и др.), а также фуллереноподобные структуры, как обособленные, так и связанные с минералами [12].
Изучение взаимодействия шунгита и цеолита с водой
Методы изучения структуры шунгита и цеолита включают СЭМ, РЭМ, дифракционный анализ, ИК-спектроскопию и др. Посредством измерения ИК-спектров в области вибрационных колебаний кристаллической решётки шунгита и цеолита можно получить информацию о структуре силикатного/алюмосиликатного каркаса, природе и локализации катионов, а также о природе структурных групп на поверхности минералов, которые являются каталитически активными сайтами [13]. Полезным методом при построении модели взаимодействия шунгита с водой является построение энергетического спектра воды, который даёт информацию о средней энергии водородных связей. Экспериментальным путём было установлено, что при испарении капли воды, угол смачивания 9 уменьшается дискретно до нуля, причём диаметр капли изменяется незначительно. Путём измерений этого угла через равные интервалы времени определяется функциональная зависимость f(θ), которая обозначается спектром состояния воды [14].
Цеолиты являются алюмосиликатными минералами натрия, калия или других элементов. Природные цеолиты образуются в условиях высоких температур и давлений при контакте вулканических пород и слоёв пепла с щелочными грунтовыми водами
Для практических целей за счёт измерения спектра состояния воды можно получить информацию об усреднённом значении энергии водородных связей в пробе воды.
Для этого используется модель У Лукка, рассматривающая воду как ассоциированную жидкость, состоящую из О-Н... О-Н групп [15]. Большая часть этих групп определяется энергией водородных связей (-E), а остальные свободны (E = 0). Функция распределения по энергиям f(E) измеряется в электронвольтах [эВ-1] и изменяется с температурой.
Для практических расчётов функции f(E) используется экспериментальная зависимость между поверхностным натяжением воды 9 и энергией водородных связей между её молекулами E:
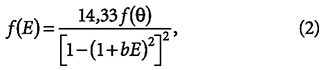
где b = 14,33 эВ-1; θ = arcos(1 – bE).
Процесс характеризуется неравновесным испарением капель воды, поэтому используется термин «неравновесный энергетический спектр воды» (НЭС).
Разность: Δf(E) = f1 - f2, где f1 — f(пробы воды); f — f (контрольной пробы воды), характеризует «дифференциальный неравновесный энергетический спектр воды» (ДНЭС). ДНЭС измеряется в миллиэлектронвольтах (мэВ) и является мерой структурных изменений воды в результате внешних воздействий.
Исследование методами НЭС и ДЭС образцов воды, полученной после трёхдневного контакта шунгита и цеолита
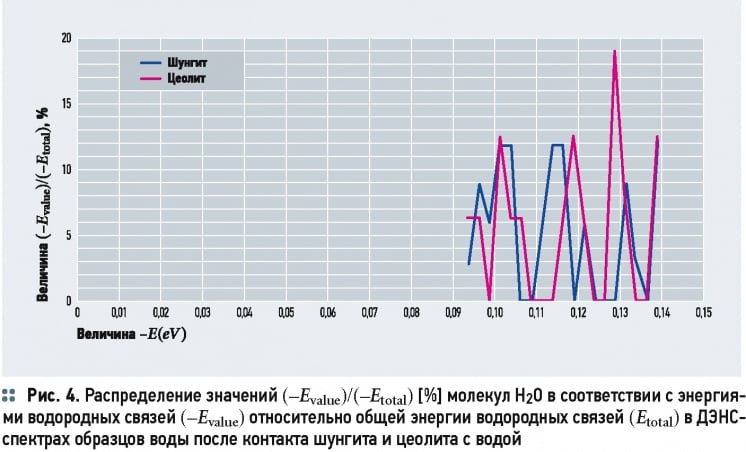
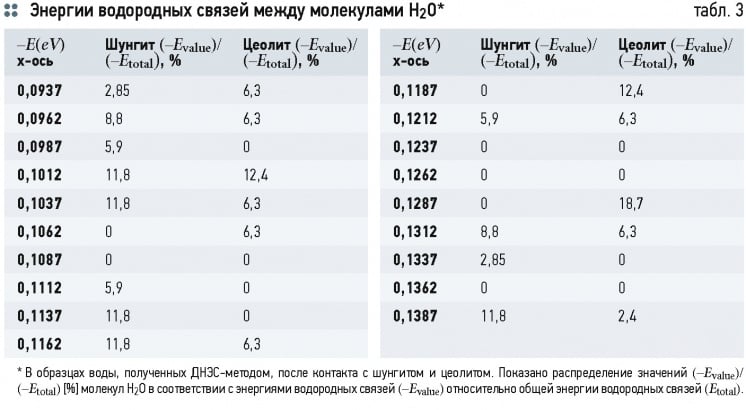
с деионизированной водой, может также дать информацию о возможном числе водородных связей в ассоциатах воды, состоящих из О-Н...О-Н групп и распределении молекул H2O по энергиям водородных связей -Evalue относительно общей энергии водородных связей Etotal в образцах воды (табл. 3).
Исследование образцов воды после трёхдневного контакта шунгита и цеолита с деионизированной водой методом ДНЭС показали значения средней энергии ΔEH-O водородных Н-О-связей между молекулами H2O, составляющие +0,0025 ± 0,0011 эВ для шунгита и -1,2 ± 0,0011 эВ для цеолита. Для контрольного образца деионизированной воды эта величина составляет -0,1162 эВ. Данная разница в значениях ΔEH-O между шунгитом и цеолитом свидетельствует о различии механизмов взаимодействия этих минералов с водой, обусловленных различным компонентным составом и структурой (пористость, плотность, адсорбционная ёмкость).
Полученные результаты свидетельствуют о реструктуризации значений энергий водородных связей между индивидуальными молекулами H2O со статистически достоверным увеличением локальных максимумов в ДНЭС-спектрах. Например, для значения 0,1387 эВ существует локальный максимум с положительным значением энергии для шунгита и цеолита.
ДНЭС-спектры водных растворов, содержащие катионы Ca2+ в концентрации 0,1 моль/л, обладали локальным максимумом энергии при -0,11 эВ и локальным минимум при -0,1 эВ. ДНЭС-спектры образцов воды после контакта с шунгитом обладают локальным максимумом энергии при -0,1137 эВ и локальным минимумом при -0,0987 эВ. При изменении температуры воды средняя энергия водородных H-O-связей в молекулах Н2О изменяется, что приводит к перераспределению молекул Н2О по энергиям в ДНЭС-спектрах [16]. По данным экспериментальным зависимостям распределения значений (-Evalue)/(-Etotal) [%] молекул H2O в соответствии с энергиями водородных связей (-Evalue) относительно общей энергии водородных связей (Etotal) в образцах воды построена математическая модель взаимодействия этих минералов с водой (рис. 3).
Выводы
Фуллеренсодержащий природный минерал шунгит и микропористый микрокристаллический алюмосиликатный минерал цеолит имеют сложную многокомпонентную структуру. Эффективность использования этих двух природных минералов обусловлена обширным спектром ценных свойств (сорбционные, каталитические, восстановительные, бактерицидные, электропроводные), экологичностью, невысокой стоимостью материалов на основе шунгита и технологий его получения и обработки, наличием обширной отечественной сырьевой базы, способствующей широкому использованию этих минералов. В результате исследований установлена математическая
модель, описывающая взаимодействие этих минералов с водой. Это позволяет понять, как эти минералы взаимодействуют с молекулами Н2О для объяснения физико-химических и адсорбционных свойств этих минералов.



























